抗生素抗性基因(ARGs)的扩散是全球公共卫生的重大威胁。污水处理厂(WWTPs)作为ARGs的关键储存库,接收来自医药、工业和城市的废水,其中活性污泥(AS)系统因微生物富集和基因水平转移(HGT)成为ARGs研究的热点。然而,既往研究多局限于局部区域或方法不一致,导致结果难以整合。2025年4月,Nature Communications(IF=16.8)上发表了题为“Global diversity and distribution of antibiotic resistance genes in human wastewater treatment systems”的文章,对六大洲142个WWTPs的226个AS样本进行宏基因组测序,首次系统揭示了全球AS中ARGs的分布规律及驱动机制。
研究覆盖六大洲的142个WWTPs,收集活性污泥样本,统一进行DNA提取、测序及质量控制。宏基因组分析:组装Contigs并预测非冗余开放阅读框(ORFs),利用CARD和ResFams数据库注释ARGs,计算丰度。通过共定位分析(<10 kb)评估ARGs与MGEs的关联,利用宏基因组组装基因组(MAGs)确定ARG宿主及水平转移潜力。采用PCoA、PERMANOVA、Procrustes分析探究ARGs与微生物群落的关系;通过归一化随机性比率(NST)和偏最小二乘(PLS)模型解析随机与确定性因素的贡献。
核心基因以四环素、β-内酰胺和糖肽类抗性基因为主。亚洲的ARG多样性显著高于其他洲,但总丰度无显著差异;ARG组成在洲际间显著分化。AS抗性组与污水、土壤相似,但与人类肠道和海洋差异显著,提示环境交互作用的影响。Chloroflexi、Acidobacteria和Deltaproteobacteria是ARGs的主要携带者,其丰度与ARGs呈强正相关。57%的MAGs携带可移动ARGs,其中65%的多菌门移动ARGs与抗生素失活机制相关,凸显HGT在抗性扩散中的作用。归一化随机性比率(NST>0.5)表明随机过程(如基因漂变)对ARG变异贡献显著。温度、城市人口与ARG丰度正相关(r=0.39),而pH、污泥停留时间则呈负相关,反映环境压力对ARGs的选择作用。本研究通过大规模标准化分析,填补了全球尺度ARGs研究的空白,为跨环境抗性管理策略提供了关键科学依据。
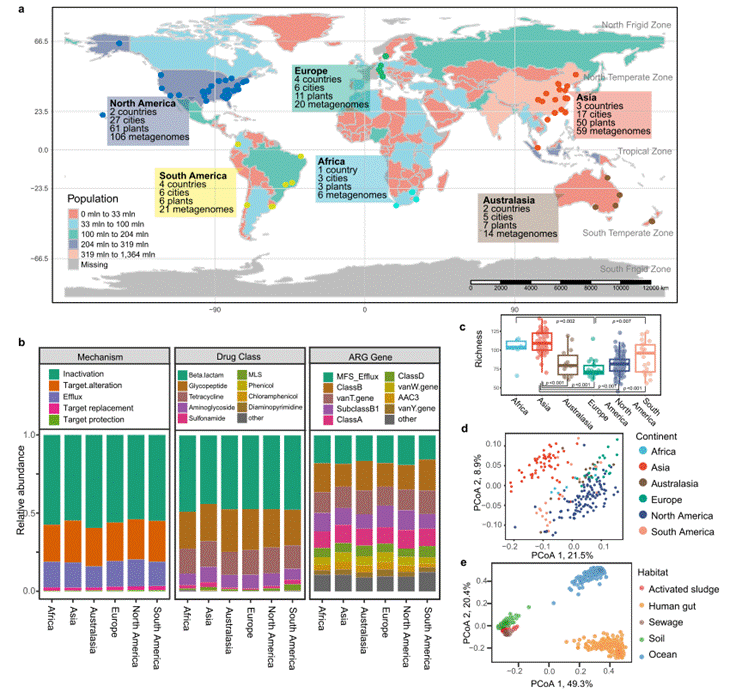
图一 AS抗性的丰度和全球分布。a)采样位置的地图;b)基于耐药机制,药物类别和九个最丰富的ARG,平均相对ARG丰度(每个细胞的ARGS副本)在不同大陆之间。 c)ARGs的丰富性。根据耐药性基因覆盖率的稀有基质计算丰富性指数,该基因覆盖范围,该基因覆盖范围,该基因被舍入并进行了采样至最低样品的水平。d)主坐标分析(PCoA)揭示了六大大洲不同的ARG组成多样性。 e)PCoA在不同环境中揭示了独特的ARG多样性。
DOI号:10.1038/s41467-025-59019-3
原文链接:https://doi.org/10.1038/s41467-025-59019-3