
由于抗生素耐药性和抗生素发现停滞,传染病是一个日益严重的全球健康威胁。特别是,对金黄色葡萄球菌感染的易感性急剧增加。耐甲氧西林金黄色葡萄球菌(MRSA)目前在美国造成的死亡人数超过艾滋病,并被疾病控制中心列为严重威胁。此外,开发新抗生素的成本和技术挑战正在增加,这突出了对替代疗法的迫切需求。免疫调节疗法作为重要的非抗生素治疗策略,已经被广泛研究。目前的免疫调节疗法,主要是基于抗体的旨在增强自身免疫系统活性,从而促进细菌的吞噬作用和清除。然而,尽管免疫调节疗法具有广阔的临床应用前景,但由于金黄色葡萄球菌感染过程和致病机制十分复杂,现阶段通过免疫调节尚无法完全应对MRSA的感染。
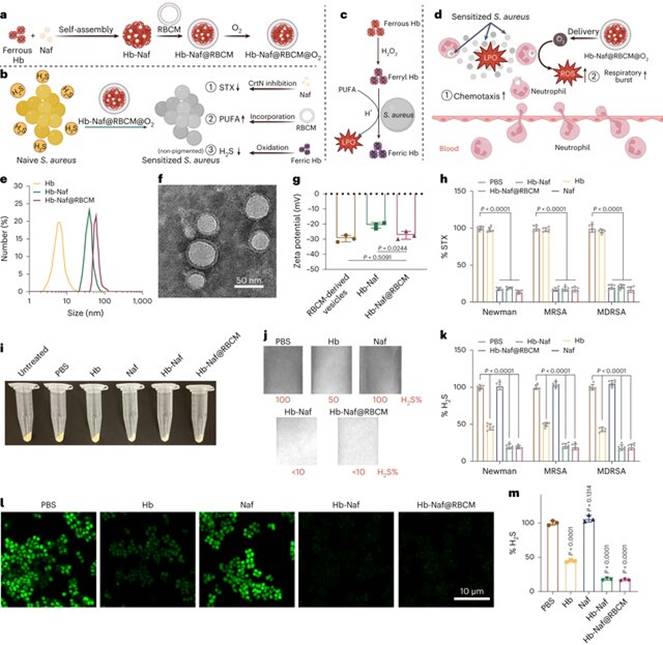
中性粒细胞是先天免疫系统抵御包括金黄色葡萄球菌在内的病原细菌的第一道防线。中性粒细胞数量与功能的异常会增加人体对金黄色葡萄球菌的易感性。尽管中性粒细胞在病原体消除中发挥着关键作用,但利用中性粒细胞杀菌活性对抗金黄色葡萄球菌的免疫疗法尚未有大量研究报道。ALS-4是一种目前正在进行临床试验的抗毒力分子。它通过抑制葡萄黄质(STX)的生物合成,使金黄色葡萄球菌对中性粒细胞介导的清除作用敏感。STX是一种起抗氧化剂作用的色素。然而,在感染MRSA的小鼠中,用ALS-4治疗仅能维持55.6%的存活率,这表明靶向单一的金黄色葡萄球菌治疗方法是不够的。此外,金黄色葡萄球菌还进化出多种抗氧化机制,包括内源硫化氢(H2S)的产生,它是一种保护金黄色葡萄菌免受宿主氧化胁迫的还原性分子。由于中性粒细胞对病原菌的清除作用主要依赖其通过呼吸爆发而造成的氧化胁迫。在缺氧感染性微环境中,中性粒细胞对金黄色葡萄球菌的清除效果会进一步收到抑制。因此,需要一种更全面的免疫疗法来提高中性粒细胞的杀菌效果。
来自威斯康星大学麦迪逊分校的Shaoqin Sarah Gong的研究团队开发一种纳米免疫疗法来对抗抗微生物耐药性的金黄色葡萄球菌感染。研究人员使用红细胞膜(RBCM)包被的纳米颗粒(NP),结合了萘替芬(Naf)和含氧血红蛋白(Hb),称为Hb-Naf@RBCMNP(图1a)。纳替芬是美国食品药品监督管理局批准的一种抗真菌药物,可抑制金黄色葡萄球菌用来逃避活性氧杀伤的STX生物合成(图1b)。金黄色葡萄球菌合成多不饱和脂肪酸(PUFA),但RBCM中的PUFA可以通过脂肪酸磷酸化整合到金黄色葡萄菌的细胞膜中,导致细菌更容易被氧化剂杀死(图1b)。在酸性和富含H2O2的感染微环境中,Hb转化为铁和铁酰Hb。铁血红蛋白催化H2S氧化并增强金黄色葡萄球菌对活性氧杀伤的敏感性。Ferryl Hb催化金黄色葡萄球菌中PUFA的脂质过氧化并产生脂质过氧化物,增强中性粒细胞的趋化性。不仅如此,纳米复合材料中的Hb可以输送分子态氧来缓解感染组织中的缺氧,恢复中性粒细胞呼吸爆发作用。这种使金黄色葡萄球菌对宿主氧化剂杀伤敏感和增强中性粒细胞募集及其氧化杀伤活性的双重策略可以显著提高感染MRSA的小鼠的存活率。该项研究不仅拓展了金黄色葡萄球菌感染防治的研究领域,更为对抗耐药型细菌感染的新型抗感染药物研发提供了新的思路和方向。
原文链接:https://www.nature.com/articles/s41565-024-01648-8